안녕하세요! 이번에 리뷰할 논문은 "Ligand-channel-enabled ultrafast Li-ion conduction, D. Lu et al., Nature, 2024, vol 627." 입니다.
이 논문에서는 독창적인 Li+ transport mechanism을 제시하며 Li+ transport ability 향상과 anion-derived SEI를 형성하게 하는 전해질 디자인에 관한 논문입니다.
Backgroud
전해질의 Li+, salt anion, solvent의 상호적인 작용이 ionic conductivity, solvation-desolvation behaviours, interphase chemistry 등 전해질의 다양한 특성을 결정합니다.
대표적으로 carbonate-based의 고리형/선형 전해질에 리튬염을 용해시킨 조합을 많이 사용하는데 저온이나 높은 전류 밀도 등 extreme condition에서 성능이 많이 저하되는 문제를 가지고 있습니다.
그에 따라, high-concentration electrolyte (HCEs), localized HCEs, weakly solvating electrolyte와 같은 대안이 연구되고 있습니다.
| HCEs | Localized HCEs | Weakly solvation electrolyte | |
| 특징 | 높은 농도의 salt | Co-solvent 이용 | Li+-solvent의 약한 결합 |
| 장점 | Solvation shell에 anion이 쉽게 접근하여 anion-derived SEI 형성 | Li+ transport 증가 | Solvation shell에 anion 접근 가능, 이동도 개선 |
| 단점 | 점도 증가로 인한 이온 전도도 감소 | 여전히 낮은 이온 전도도 | 너무 작은 solvating ability은 dissociation이 어려움 |
아래 그림 1을 보겠습니다.

일반적으로 dilute electrolyte에선(그림 1. (a)) Li+가 solvent molecule에 둘러쌓여 solvation shell을 형성하여 이동합니다.
HCEs에서는 그림 1.(b)와 같이 Li+가 다양한 anion/solvent envrionment에서 가능한 다양한 배위결합을 통해 이동하는데 이것은 높은 에너지 장벽을 가지고 있어 리튬 이온 이동도 저하의 원인이 됩니다.
이 논문에서는 Li+와 solvent 사이의 낮은 solvation energy를 유지하며(너무 낮으면 lithium salt의 완전한 dissociation을 불가능하게 만들어 Li-ion conductivity가 감소합니다.) 높은 ionic conductivity를 갖음으로써, Li+ transport 향상과 anion-derived SEI 형성을 목표로 하는 전해질 설계에 대한 통찰력을 제공합니다.
Small-sized solvent with weak solvation energy and high Li-ion conductivity
- Solvent screening
먼저 여러 solvent 중 낮은 solvation energy를 갖는 solvent를 스크리닝합니다.
Solvation energy는 Li+가 solvent와 결합할 때 방출되는 에너지입니다. |solvation energy|가 클수록 강한 결합을 합니다.


그림 2(a)를 보면 파란색 부분이 낮은 solvation energy를 갖아 후보를 추릴 수 있습니다.
또한 아래 식을 통해 Li-ion conductivity가 크기 위해선 Etrans가 작고 VNs (shell volume)이 작아야 한다는 것을 알 수 있습니다.

그렇게 추려낸 solvent 분자가 그림 2(b)에 표시되어 있습니다.
그러나 물 분자는 solvation energy가 커 solvation shell에 anion이 존재하지 못하고, 좁은 전기화학창(1.23 V)은 고에너지 LIB적용에 어려움이 있습니다.
AN solvent는 낮은 환원 안정성을 보여 FAN solvent가 최종적으로 선택되었습니다.
- Li+ transport mechanism
아래 그림 3을 보게 되면 FAN, AN solvent는 다른 solvent보다 Li+-solvent cluster에서 Li+와의 결합 길이가 상대적으로 더 긴 것을 확인할 수 있습니다.

이는 다른 solvent에 비해 상대적으로 약한 배위 결합을 형성하여 빠른 리간드 교환 반응에 의해 Li+의 이동도가 빠르다는 것을 알 수 있습니다.
따라서 Li+ transport mechanism은 그림 4처럼 작은 solvent 분자들이 2nd solvation shell을 형성하고, 이 solvent 분자들이 내부의 Li+와 지속적으로 상호 작용을 하며 solvation structure을 재조정하며 빠르게 Li+을 이동시키는 것입니다.

- At extreme conditions
다음으로 고농도의 염을 사용했을 때와 극한 온도 범위에서의 이온 전도도에 대하여 알아보겠습니다.
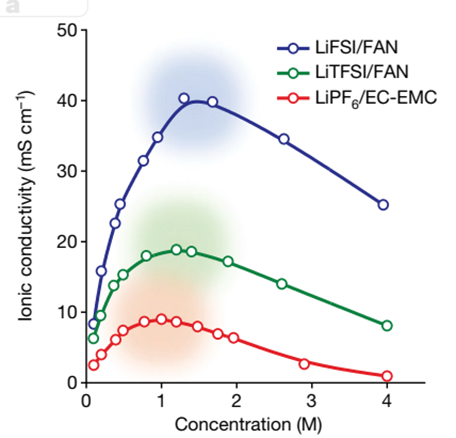
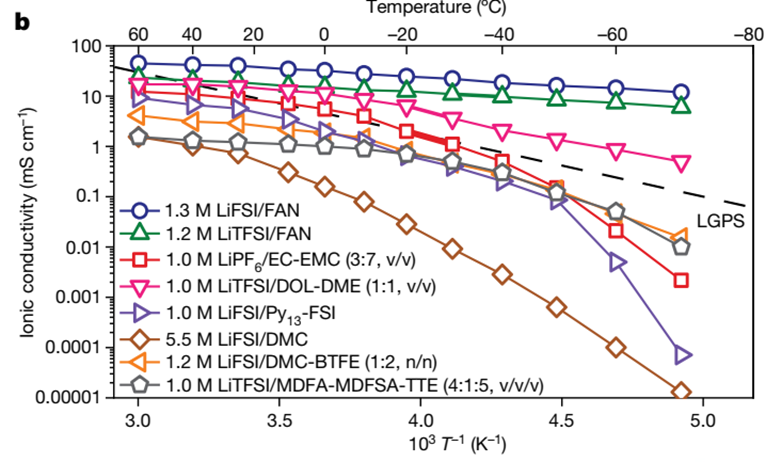
위 그림 5에서 볼 수 있듯이, LiFSI/FAN 조합은 염농도를 증가시켜도 이온 전도도가 높다는 것을 알 수 있습니다.
또한, FAN solvent는 저온의 환경에서도 다른 solvent에 비해 높은 이온 전도도를 보이는 것을 알 수 있습니다.
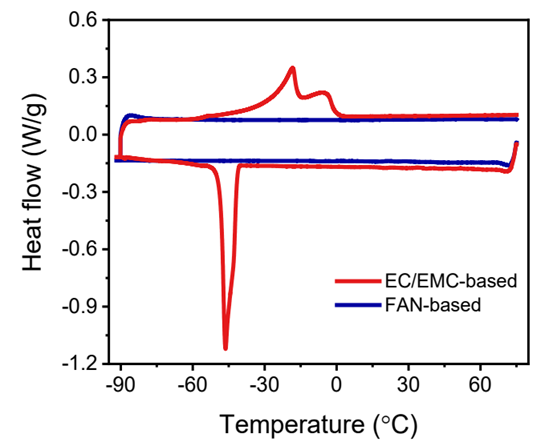
Carbonate-based electrolyte는 -20 ℃에서 solidification을 보여 급격한 이온 전도도 감소를 보입니다.
그러나, FAN-based electrolyte는 -90 ℃까지도 여전히 액체상태를 유지하는 것을 알 수 있습니다 (그림 6).
또한, 논문에 보면 FAN-based는 다른 조합에 비해 낮은 점도를 보이는 것을 확인할 수 있습니다.
전해질에서 H-bond가 증가하면 점도가 증가합니다. 점도가 증가하면 Stokes-Einstein equation에 의해 diffusivity도 감소하고 따라서 이온 전도도가 감소하게 됩니다.
아래 그림 7을 보면 FAN 분자는 홀로 있을 때에 비해 리튬염과 존재할 때 Raman spectra에서 H-bond의 세기가 감소하는 것을 확인할 수 있습니다.
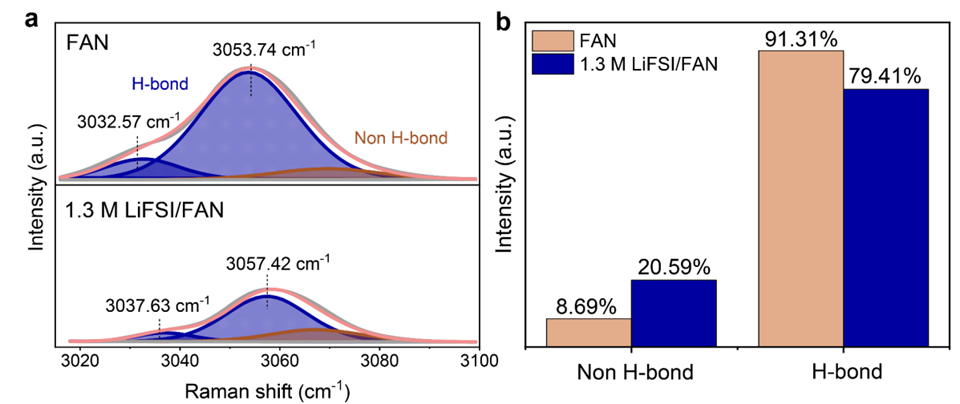
즉, 점도가 낮아 리튬 이온의 이동이 원활해지고, 따라서 높은 이온 전도도를 보입니다.
이번 논문은 많이 축약하려 했음에도 내용이 많아 (1), (2)로 나누어 포스팅하겠습니다!
이번 포스팅은 여기까지 하도록 하겠습니다.
Reference)
D. Lu et al., Nature, 2024, vol 627.
※ 참고해주세요
※ 아직 많이 부족한 학생의 개인 공부용 포스팅입니다.
※ 포스팅은 특성 상 많은 내용을 생략합니다. 내용에 관심이 간다면 reference를 참조하여 읽어주세요.
※ 공감은 힘이 됩니다..!! 감사합니다!
※ 저작권의 문제가 있을 시 수정 및 삭제하겠습니다.